肼(N2H4)是氮和氢形成的一种化合物,易溶于水.工业上利用尿素法生产肼,同时得到副产品十水合碳酸钠,其工艺流程如下:十水合碳酸钠制肼过程的反应为:CO(NH2)2(尿素)+NaClO+2NaOH=N
发布时间:2019-08-07 20:36:53
试题难度:难度:偏易 试题类型:填空题 试题内容:肼(N2H4)是氮和氢形成的一种化合物,易溶于水.工业上利用尿素法生产肼,同时得到副产品十水合碳酸钠,其工艺流程如下:
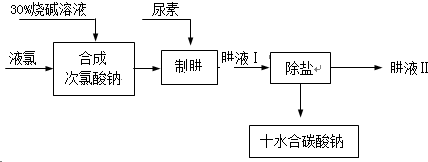
十水合碳酸钠制肼过程的反应为:CO(NH2)2(尿素)+NaClO+2NaOH=N2H4+Na2CO3+NaCl+H2O.
(1)实验室若配制30%烧碱溶液,所需的玻璃仪器除玻璃棒外,还有______(选填编号).
A.漏斗 B.烧杯 C.烧瓶 D.量筒
(2)已知:Cl2+H2O=HCl+HClO,请推测Cl2与NaOH溶液发生反应的化学方程式:______.
从后续反应过程来看,若要使原料不浪费,合成次氯酸钠时投入的液氯与烧碱的质量之比为71:______.
(3)在实验室中,欲从母液中分离出十水合碳酸钠晶体.可采用的操作依次为______(选填编号).
A.蒸馏 B.蒸发 C.灼烧 D.过滤 E.冷却结晶
(4)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧等.请写出肼除氧时发生反应的化学方程式:______.

十水合碳酸钠制肼过程的反应为:CO(NH2)2(尿素)+NaClO+2NaOH=N2H4+Na2CO3+NaCl+H2O.
(1)实验室若配制30%烧碱溶液,所需的玻璃仪器除玻璃棒外,还有______(选填编号).
A.漏斗 B.烧杯 C.烧瓶 D.量筒
(2)已知:Cl2+H2O=HCl+HClO,请推测Cl2与NaOH溶液发生反应的化学方程式:______.
从后续反应过程来看,若要使原料不浪费,合成次氯酸钠时投入的液氯与烧碱的质量之比为71:______.
(3)在实验室中,欲从母液中分离出十水合碳酸钠晶体.可采用的操作依次为______(选填编号).
A.蒸馏 B.蒸发 C.灼烧 D.过滤 E.冷却结晶
(4)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧等.请写出肼除氧时发生反应的化学方程式:______.
推荐回答
试题答案:(1)配制溶液需要在烧杯内进行,需要用量筒量取水,用玻璃棒搅拌,还用到胶头滴管,所以选择BD;(2)由Cl2+H2O=HCl+HClO,可知Cl2与NaOH溶液发生反应时,氯气先与水反应,生成的盐酸、次氯酸再与氢氧化钠反应生成氯化钠、次氯酸钠和水,所以反应物是氯气和氢氧化钠,生成物是氯化钠、次氯酸钠和水,用观察法配平即可,所以方程式是:Cl2+2NaOH=NaCl+NaClO+H2O;根据氯气和氢氧化钠反应的方程式可知:投入的液氯与烧碱的质量之比为:35.5×2:2×40=71:80;(3)碳酸钠的溶解度随温度变化比较大从溶液中结晶析出的方法:冷却热饱和溶液的方法,所以先将溶液加热蒸发,再降温,使晶体析出,再进行过滤,所以步骤为:BED.(4)肼除氧的反应物是肼和氧气,因为氧化产物无污染所以是氢和氧结合成的水,根据质量守恒定律可知生成物还有氮气,再根据观察法配平,所以方程式是:N2H4+O2=N2+2H2O.故答案为:(1)BD;(2)Cl2+2NaOH=NaCl+NaClO+H2O;80;(3)BED;(4)N2H4+O2=N2+2H2O.以上问题属网友观点,不代表本站立场,仅供参考!
- 上一条:某校学生对买来的工业固体烧碱
- 下一条:在化工生产中,原料往往不能全部