某含镍(Ni)废催化剂中主要含有Ni,还含有Al、Al_2O_3、Fe及其他不溶于酸、碱的杂质.部分阳离子以氢氧化物形式完全沉淀时溶液的pH如下:沉淀物Al(OH)_2Fe(OH)_3Fe(OH))_
发布时间:2019-08-07 01:08:07
某含镍(Ni)废催化剂中主要含有Ni,还含有Al、Al2O3、Fe及其他不溶于酸、碱的杂质.部分阳离子以氢氧化物形式完全沉淀时溶液的pH如下:
Ni (OH)2 PH 5.2 3.2 9.7 9.2
欲从含镍废催化剂中制得NiSO4•7H2O晶体,其流程如下: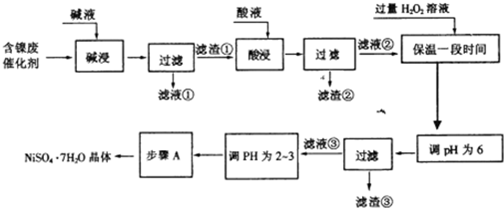
请根据以上信息和流程图,回答下列问题:
(1)“碱浸”的目的是除去含镍废催化剂中的______.
(2)“酸浸”时所加入的酸是_______.酸浸后,滤液②中可能含有的金属离子是______.(用离子符号表示).
(3)“调pH为2-3的目的是______.
(4)步骤A的操作顺序是加热浓缩、冷却、______、______.
(5)NiSO4在强碱溶液中用NaC1O氧化,可制得碱性镍镉电池电极材料NiOOH.该反应的离子方程式为______.
推荐回答
解:(1)“碱浸”过程中是为了除去铝及其氧化物,铝和氧化铝都可以和强碱反应溶解得到偏铝酸盐,反应的离子方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑、Al2O3+2OH-═2AlO2-+3H2O,故答案为:Al、Al2O3;(2)“酸浸”时主要是溶解镍金属和铁单质及其氧化物,依据制备目的是得到NiSO4•7H2O,加入的酸不能引入新的杂质,所以需要加入硫酸进行酸浸;镍、铁和稀硫酸反应生成硫酸亚铁、硫酸镍溶液,故答案为:H2SO4;Ni2+、Fe2+;(3)硫酸镍溶液需要蒸发浓缩结晶析出,为防止镍离子水解生成氢氧化镍沉淀,需要控制溶液pH,故答案为:防止在浓缩结晶过程中Ni2+水解;(4)步骤A的操作顺序是加热浓缩、冷却、结晶、过滤,故答案为:结晶、过滤;(5)NiSO4在强碱溶溶中用NaClO氧化,可制得碱性镍镉电池电极材料--NiOOH.该反应的离子方程式是:2Ni2++ClO-+4OH-=2NiOOH+Cl-+H2O,故答案为:2Ni2++ClO-+4OH-=2NiOOH↓+Cl-+H2O.以上问题属网友观点,不代表本站立场,仅供参考!
- 上一条:下列事实不能用勒夏特列原理解
- 下一条:下列事实中,不能用勒夏特列原理