(14分)镁、铝是两种重要的金属,它们的单质及化合物有着各自的性质。Ⅰ.海水中含有氯化镁,是镁的重要来源之一。从海水中制取镁,某同学设计了如下流程步骤:主要的步骤总结如下:①把贝壳制成石灰乳 ②往母液
发布时间:2019-08-07 18:41:03
试题难度:难度:中档 试题类型:填空题 试题内容:(14分)镁、铝是两种重要的金属,它们的单质及化合物有着各自的性质。
Ⅰ.海水中含有氯化镁,是镁的重要来源之一。从海水中制取镁,某同学设计了如下
流程步骤:
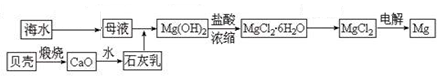
主要的步骤总结如下:①把贝壳制成石灰乳 ②往母液中加石灰乳,沉降、过滤,得到Mg(OH)2沉淀 ③将沉淀物与盐酸反应,结晶、过滤,将制得的晶体脱水得无水MgCl2
④将得到的产物熔融后电解。
(1)下列说法不正确的是__________________(填代号)A.此法的优点之一是原料来源丰富B.进行①②③步骤的目的是从海水中提取氯化镁C.第④步电解法制取镁是由于镁是很活泼的金属D.以上制取镁的过程中涉及的反应有分解反应、化合反应和置换反应(2)步骤②不够合理,理由是
Ⅱ.(1)铝、空气、海水可组成一种电池,广泛用于制造航标灯。此电池正极的电极反应为 。
(2)铝热还原法是冶炼熔点较高的金属的一种重要方法,焊接钢轨即用到此法。将干燥的氧化铁粉末和铝粉均匀混合后放入纸漏斗中(漏斗已事先处理好),并架在铁架台上,
下面放置一个盛有沙子的蒸发皿。请写出引发铝热反应的操作及该反应的化学方程式:
操作
化学方程式 。
(3)为确定某铝热剂(氧化铁粉末和铝粉)的组成,分别进行下列实验。
若取10.7g样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况)体积为3.36L,反应的化学方程式为 ,样品中铝的质量是 g。
若取10.7g样品将其点燃,恰好完全反应,待反应产物冷却后,加入足量盐酸,测得生成的气体体积为aL,该气体与上小题中所得气体的体积比等于 ∶ 。
Ⅰ.海水中含有氯化镁,是镁的重要来源之一。从海水中制取镁,某同学设计了如下
流程步骤:

主要的步骤总结如下:①把贝壳制成石灰乳 ②往母液中加石灰乳,沉降、过滤,得到Mg(OH)2沉淀 ③将沉淀物与盐酸反应,结晶、过滤,将制得的晶体脱水得无水MgCl2
④将得到的产物熔融后电解。
(1)下列说法不正确的是__________________(填代号)A.此法的优点之一是原料来源丰富B.进行①②③步骤的目的是从海水中提取氯化镁C.第④步电解法制取镁是由于镁是很活泼的金属D.以上制取镁的过程中涉及的反应有分解反应、化合反应和置换反应(2)步骤②不够合理,理由是
Ⅱ.(1)铝、空气、海水可组成一种电池,广泛用于制造航标灯。此电池正极的电极反应为 。
(2)铝热还原法是冶炼熔点较高的金属的一种重要方法,焊接钢轨即用到此法。将干燥的氧化铁粉末和铝粉均匀混合后放入纸漏斗中(漏斗已事先处理好),并架在铁架台上,
下面放置一个盛有沙子的蒸发皿。请写出引发铝热反应的操作及该反应的化学方程式:
操作
化学方程式 。
(3)为确定某铝热剂(氧化铁粉末和铝粉)的组成,分别进行下列实验。
若取10.7g样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况)体积为3.36L,反应的化学方程式为 ,样品中铝的质量是 g。
若取10.7g样品将其点燃,恰好完全反应,待反应产物冷却后,加入足量盐酸,测得生成的气体体积为aL,该气体与上小题中所得气体的体积比等于 ∶ 。
推荐回答
试题答案:(14分)Ⅰ.(1)D (1分)(2)石灰乳中的Ca(OH)2为微溶物,制得的Mg(OH)2不纯净。(1分)Ⅱ.(1)(1)O2 + 4e-+2H2O 4OH-(2分)(2)在混合物上面加入少量氯酸钾固体,中间插入一根用砂纸打磨过的镁条并点燃镁条。(2分) 2Al+Fe2O3Al2O3+2Fe (2分)(3)2Al+2NaOH+2H2O==2NaAlO2+3H2↑ (2分) 2.7 (2分) 2:3 (2分以上问题属网友观点,不代表本站立场,仅供参考!
- 上一条:课外化学兴趣小组的同学利用某
- 下一条:某小组用碳酸钠和石灰乳来制备