九年级化学题目
发布时间:2019-08-07 19:27:12
为测定锌铜合金中锌的含量,取该合金放入盛有稀硫酸的锥形瓶中(如下图),发生反应。(铜与稀硫酸不反应)多次试验后,取平均值所得数据如下表:
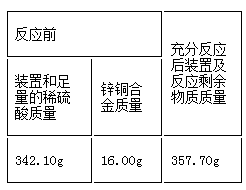
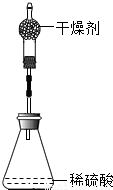
若不考虑干燥剂吸收空气中的水蒸气,计算该合金中铜的质量
推荐回答
还没有选出推荐答案,请稍候访问或查看其他回答!其他回答
根据质量守恒定律,反应前后质量总和相等,即342.10+16.00=357.70+氢气质量,算得氢气质量=0.4g
利用化学方程式H2SO4+Zn==ZnSO4+H2,算的锌的质量为13g
因此铜的质量=16-13=3g
用差量法,减轻的质量是生成的氢气的质量,
H2SO4 +Zn==ZnSO4 +H2
65 2
X 342.10+16.00-377.70,X=13,铜的质量=16-13=3克请采纳,
以上问题属网友观点,不代表本站立场,仅供参考!
- 上一条:初三化学题。题目如图
- 下一条:奶牛粪的氮磷钾含量