(13分)Ⅰ.某学校研究性学习小组开展“不同条件对化学反应速率影响的探究”课题,选用4mL0.01mol·L-1KMnO4溶液与2mL0.1mol·L-1H2C2O4溶液进行实验,改变条件如下:组别1
发布时间:2019-08-07 04:44:05
试题难度:难度:中档 试题类型:实验题 试题内容:(13分)Ⅰ.某学校研究性学习小组开展“不同条件对化学反应速率影响的探究”课题,选用4 mL 0.01 mol·L-1KMnO4溶液与2 mL 0.1 mol·L-1 H2C2O4溶液进行实验,改变条件如下:
组别
10%硫酸的体积(mL)
温度/℃
其他物质
①
2 mL
20
②
2 mL
20
10滴饱和MnSO4溶液
③
2 mL
30
④
1 mL
20
1 mL蒸馏水
(1)如果研究催化剂对化学反应速率的影响,使用实验 和 (用①~④表示,下同);如果研究温度对化学反应速率的影响,使用实验 和 。
(2)对比实验①和④,可以研究 对化学反应速率的影响,实验④中加入1 mL蒸馏水的目的是 。
Ⅱ.该小组查阅资料得知:C2O42-+MnO4-+H+→ CO2↑+Mn2++H2O(未配平),欲利用该反应测定某草酸钠(Na2C2O4)样品中草酸钠的质量分数。该小组称量1.34 g草酸钠样品溶于稀硫酸中,然后用0.200 mol·L-1的酸性高锰酸钾溶液进行滴定(其中的杂质不跟高锰酸钾和稀硫酸反应)。
(1)滴定前是否要滴加指示剂? (填“是”或“否”),请说明理由 。
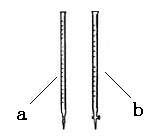
(2)滴定时用 (填a或b)滴定管盛装KMnO4标准溶液。
(3)达到终点时消耗了15.00 mL的高锰酸钾溶液,样品中草酸钠的质量分数为 。
组别
10%硫酸的体积(mL)
温度/℃
其他物质
①
2 mL
20
②
2 mL
20
10滴饱和MnSO4溶液
③
2 mL
30
④
1 mL
20
1 mL蒸馏水
(1)如果研究催化剂对化学反应速率的影响,使用实验 和 (用①~④表示,下同);如果研究温度对化学反应速率的影响,使用实验 和 。
(2)对比实验①和④,可以研究 对化学反应速率的影响,实验④中加入1 mL蒸馏水的目的是 。
Ⅱ.该小组查阅资料得知:C2O42-+MnO4-+H+→ CO2↑+Mn2++H2O(未配平),欲利用该反应测定某草酸钠(Na2C2O4)样品中草酸钠的质量分数。该小组称量1.34 g草酸钠样品溶于稀硫酸中,然后用0.200 mol·L-1的酸性高锰酸钾溶液进行滴定(其中的杂质不跟高锰酸钾和稀硫酸反应)。
(1)滴定前是否要滴加指示剂? (填“是”或“否”),请说明理由 。
(2)滴定时用 (填a或b)滴定管盛装KMnO4标准溶液。

(3)达到终点时消耗了15.00 mL的高锰酸钾溶液,样品中草酸钠的质量分数为 。
推荐回答
试题答案:Ⅰ.(1)①和② (1分) ; ①和③ (1分)(2)硫酸的浓度或氢离子浓度(2分); 确保①和④组对比实验中c(KMnO4)、c(H2C2O4)浓度不变或确保溶液总体积不变 (2分)Ⅱ.(1)否 ,KMnO4溶液呈紫色,达滴定终点紫色不再褪去。(2分)(2)b (2分) (3)75% (3分)以上问题属网友观点,不代表本站立场,仅供参考!
- 上一条:(1)下列条件对化学反应速率可
- 下一条:I.下列四支试管中,过氧化氢分解